Profesor Hazem M. Kalaji z Instytutu Biologii SGGW oraz dr. Seiya Sato światowej sławy wirusolog z Japonii opracowali i opatentowali substancję zapobiegającą infekcjom koronawirusem. Może być ona stosowana w postaci cukierków, lizaków, gum do żucia, napojów lub płynów do płukania jamy ustnej, gardła i krtani.
Koronawirusy, w tym SARS-CoV-2, nadal stanowią poważne zagrożenie dla zdrowia publicznego. Patent (o numerze JP,2023-143850,A; numer aplikacji: JP,2023-045934) prof. dr. hab. Hazema M. Kalajiego ze Szkoły Głównej Gospodarstwa Wiejskiego oraz Jego wspólnika Dr. Seiya Sato z Japonii, został opublikowany 6 października 2023 roku przez Japoński Urząd Patentowy (JPO):
Celem opracowania wynalazku było stworzenie skutecznych środków zapobiegających zakażeniu koronawirusem, które nie wymagają podawania drogą iniekcji, jednocześnie można je produkować prostą i ekonomiczną metodą oraz są zdolne do efektywnego hamowania bardzo zakaźnych chorób, w tym ostatnio wykrytej choroby wywołanej koronawirusem.
Przypomnijmy, że w 2021 r. dr S. Sato wraz z prof. H. Kalajim opublikowali ich pierwszy patent dotyczący opracowania półmaski antywirusowej z mchów (biologicznie aktywna półmaska).
Więcej: https://media.sggw.pl/aktualnosci/716065/polmaska-antywirusowa-z-mchow
Opis patentu:
Ostatnio zaobserwowano częstsze epidemie nowo odkrytych zakażeń wirusowych, które pojawiają się nagle i szybko się rozprzestrzeniają, zwłaszcza w określonej populacji i regionach świata, gdzie istnieją duże możliwości kontaktu między ludźmi a zwierzętami. Mimo dostępności wielu metod leczenia opracowanie nowych sposobów terapii zajmuje kilka lat, a ze względu na coraz większe przemieszczanie się ludzi, zakażenie rozprzestrzenia się w krótkim czasie co stanowi duży problem na całym świecie.
Dotychczas główną metodą zapobiegania zakażeniom wirusowym jest pobudzanie odporności komórkowej poprzez szczepienia, które wzmacniają barierę obronną organizmu. Opracowanie skutecznych i bezpiecznych szczepionek jest koszto- i czasochłonne. Epidemia SARS (zespół ostrej ciężkiej niewydolności oddechowej) skłoniła do opracowania szczepionki na tę chorobę. Nie została ona jednak wprowadzona do praktycznego użytku ze względu na ograniczenie rozprzestrzeniania się zakażenia i ze względów ekonomicznych, szczególnie że choroba w dużej mierze dotyczyła ubogich krajów (szczepionki przeciwko COVID-19 zostały opracowane na potrzeby walki z pandemią COVID-19).
Zaszczepienie społeczeństwa wymaga dużych nakładów finansowych oraz zaangażowania ogromnej liczby osób. Dlatego istnieje duże zapotrzebowanie na alternatywne środki zapobiegawcze, które są prostsze i tańsze w zastosowaniu niż szczepienia, a zarazem wykazują skuteczność w tłumieniu zakażeń COVID-19.
W ramach poszukiwania alternatywnych naturalnych sposobów do walki z wirusami, naukowcy podjęli się badań nad wykorzystaniem substancji wykazujących działania antywirusowe zawartych w roślinach. Dzięki badaniom prof. Kalajiego i jego wspólnika dr. Sato okazało się, że kanawalia szablasta, roślina z rodziny bobowatych, zawiera konkanawalinę A (ConA), która może posłużyć się do stworzenia prostego i taniego rozwiązania do walki z wirusami.
https://pl.wikipedia.org/wiki/Kanawalia_szablasta
Kanawalia szablasta jest uprawiana głównie na terenie Afryki, Azji Południowej, USA i na Antylach. Dotychczas roślinę spożywano jako jarzynę w postaci niedojrzałych strąków. W stanie dojrzałym nasiona wykazują działanie trujące. Roślina jest również uprawiana jako zielony nawóz.
Konkanawalina A, skrótowo nazywane Con A, to białko występujące w nasionach rośliny z rodziny bobowatych, często nazywanej “Jack Bean“. Konkanawalina A jest popularnym narzędziem wykorzystywanym w biochemii i biologii molekularnej ze względu na swoją zdolność do wiązania się z cukrami i glikoproteinami, co ma wiele zastosowań w badaniach naukowych i medycynie.
Konkanawalina A (ConA) cechuje się wysokim powinowactwem do białka wystającego z zewnętrznej otoczki wirusa oraz składnika zasadowego. Można ją podawać doustnie, aby ograniczyć zakaźność wirusa w obrębie jamy ustnej, gardła lub krtani, co ogranicza dalsze przenikanie wirusa do komórek nabłonka dróg oddechowych lub pęcherzyków płucnych. Działanie takie ogranicza jego namnażanie się.
ConA może wiązać się z białkiem kolca wystającym z zewnętrznej powłoki koronawirusa i fizycznie ograniczać patogenowi zdolności przyłączenia się do receptora wirusa na powierzchni komórki gospodarza. Zaletą tej substancji jest roślinne pochodzenie, a przez to może być stosowana w bezpieczny i masowy sposób. Podawanie ConA doustnie razem z komponentem alkalicznym pozwala na osiągnięcie bardzo wysokiego efektu hamowania infekcji wirusowej dzięki synergicznemu działaniu wiązania koronawirusa przez ConA i dezaktywacji patogenu w środowisku alkalicznym.
Jednym z wariantów wynalazku jest opracowanie zestawienia (składu) zawierającego te substancje, umożliwiającego optymalne hamowanie infekcji koronawirusem. Stężenie konkanawaliny A (ConA) mieści się w zakresie od 20 do 80 μg/ml, a poziom pH mieści się w zakresie od 9,0 do 11,0.
Tak opracowany wynalazek podawany jest doustnie. Jest rozcieńczany śliną lub podobnymi substancjami, a następnie stosowany w taki sposób, aby pH w części lub na całej powierzchni jamy ustnej, gardła lub krtani mieściło się w określonym zakresie (od 9,0 do 11,0). W tej opracowanej procedurze poziom pH roztworu wynosi powyżej 8,5. Wiadomo jest, że białka ulegają denaturacji w pH 12,0 lub powyżej, w zależności od stopnia jonizacji i rozpuszczalności związków alkalicznych, i uważa się, że taki odczyn mógłby wpływać negatywnie na błony śluzowe i tkanki. Dlatego roztwory o pH 12,0 lub więcej nie są zalecane, a zasadowy odczyn o pH 11 lub mniej może mieć największą przeciwwirusową aktywność.
Zawartość ConA w formie niniejszego wynalazku jest opracowana w taki sposób, aby po podaniu doustnym uzyskać wyżej opisane określone stężenie roztworu z zachowaniem akceptowalnego smaku i zapachu. Wynalazek ten może być stosowany w formie twardych cukierków o kształcie zbliżonym do kulistego i wadze 4 g. Można założyć, że czas rozpuszczania takiego produktu w jamie ustnej wynosi 10 minut. Przy założeniu, że ilość śliny w jamie ustnej wynosi 2,5 mL, a ilość wydzielania śliny po podaniu doustnym wynosi 4 mL/minutę. Zawartość ConA względem całkowitej ilości składnika cukierkowego powinna wynosić, co najmniej 0,016%. Im większa zawartość tej substancji, tym działanie wynalazku będzie bardziej skuteczne. Preferowana zawartość mieści się w zakresie 0,033 – 0,13%.
Żywotność hodowli komórek traktowanej każdym stężeniem ConA zmierzono za pomocą metody barwienia (metoda MTT), w celu określenia efektu przeciwwirusowego. Test ten wykorzystywał trzy komory na próbkę (w trzech powtórzeniach). Gdy stężenie ConA wynosiło 0 μg/mL, żywotność komórek niezainfekowanych wynosiła 100%, a żywotność komórek zakażonych wynosiła 0%, co stanowiło punkt odniesienia do oceny efektu hamującego ConA na śmierć komórek wywołaną przez wirusa. Wyniki przedstawione są w Tabeli 1 i Rysunku 3.
Tabela 1.
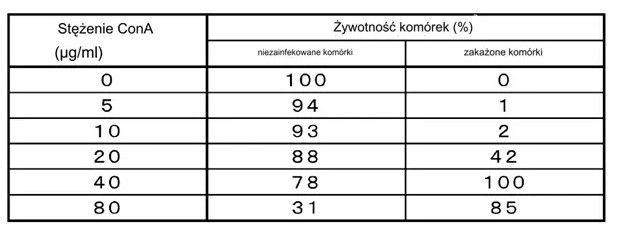
Efekt przeciwwirusowy ConA został potwierdzony w innym doświadczeniu w taki sam sposób jak w Przykładzie 1, z wyjątkiem tego, że gdy SARS-CoV-2 został zainokulowany do hodowanych komórek VeroE6, przy różnym pH roztworów uzyskiwanych poprzez dodanie 0,01 N roztworu wodnego hydroksydu sodu, co przedstawiono w Tabeli 2 i Rysunku 4.
Tabela 2.
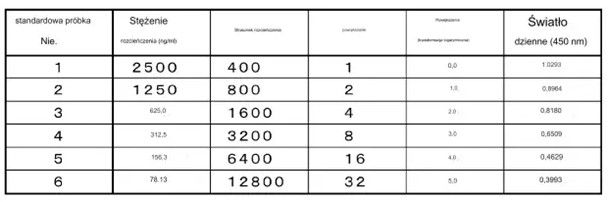
Aby przygotować krzywą kalibracyjną, roztwór ConA przeznaczony do badań biochemicznych (wyprodukowany przez FUJIFILM Wako Pure Chemical Industries, Ltd., kod produktu: 031 do 08774) został rozcieńczony w PBS uzyskując różne stężenia co przedstawiono w Tabeli 3.
Roztwór substancji zawartych w cukierku został rozcieńczony 14-krotnie w PBS w taki sposób, aby stężenie ConA wynosiło 40 μg/mL. W tym przypadku stosowano 0,01N roztwór wodnego hydroksydu sodu do uzyskania odpowiedniego poziomu pH roztworu zawartych w cukierku (od 7,5 do 10,0). Przy użyciu roztworów substancji zawartych w cukierku o różnym pH potwierdzono efekt przeciwwirusowy ConA w taki sam sposób jak w Przykładzie 1. Wyniki przedstawiono w Tabeli 4. W teście z użyciem proszku z fasoli (Jack bean), podobnie jak w przypadku oczyszczonego ConA, zaobserwowano wysoki efekt hamowania infekcji przez koronawirusa nowej generacji. W szczególności przy pH9 lub wyższym zaobserwowano efekt hamowania infekcji na poziomie około 95% lub wyższym.
Tabela 4.

W roztworze testowym A na początku testu zaobserwowano ilość wirusa wynosząca 106,3 TCID50/mL, a po 120 minutach po rozpoczęciu testu zaobserwowano <102,5 TCID50/mL (mniej niż limit ilościowy). W roztworze testowym B zaobserwowano naturalny spadek (120 → 106,1 TCID50/mL) ilości wirusa od początku testu do 106,3 po rozpoczęciu. Z przeprowadzonych badań wynika, że w części testowej, w której użyto materiału testowego, w porównaniu do części kontrolnej, w której materiał testowy nie był używany, zaobserwowano redukcję zakaźności wirusa wynoszącą 9,97% lub więcej. Wyniki przedstawiono w Tabeli 5 poniżej.
Stopień redukcji miana zakażonego wirusa (TCID50/ml)

Rysunki:
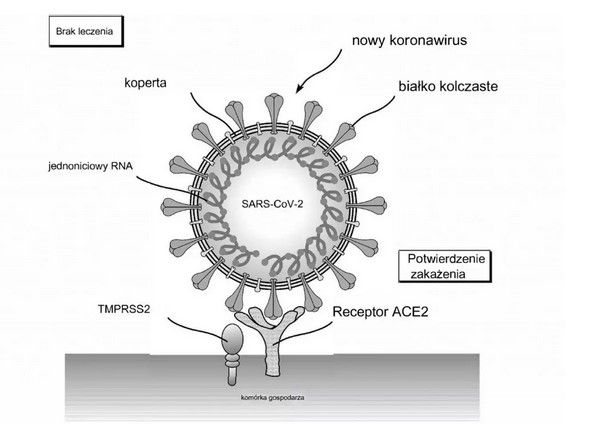
Rysunek 1. schemat objaśniający/przedstawiający strukturę wirusa i wiązanie z receptorem wirusa.
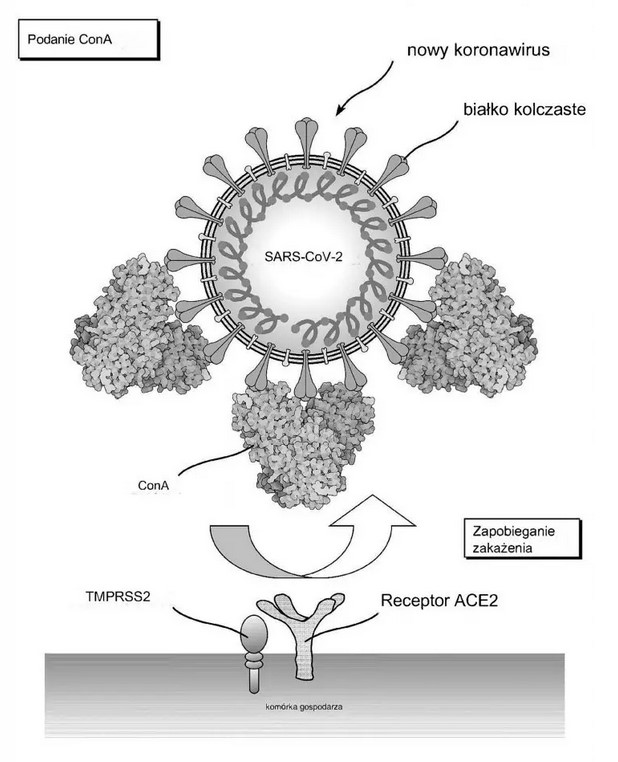
Rysunek 2. Diagram wyjaśniający/przedstawiający mechanizm działania przeciwwirusowego działania konkanawaliny A (Con A).
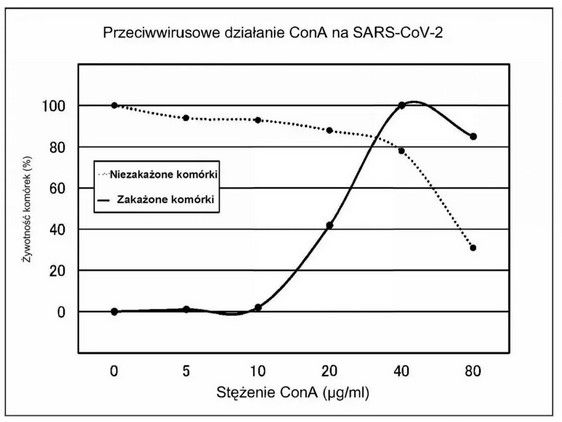
Rysunek 3. Przeciwwirusowy wpływ ConA na SARS-CoV-2.
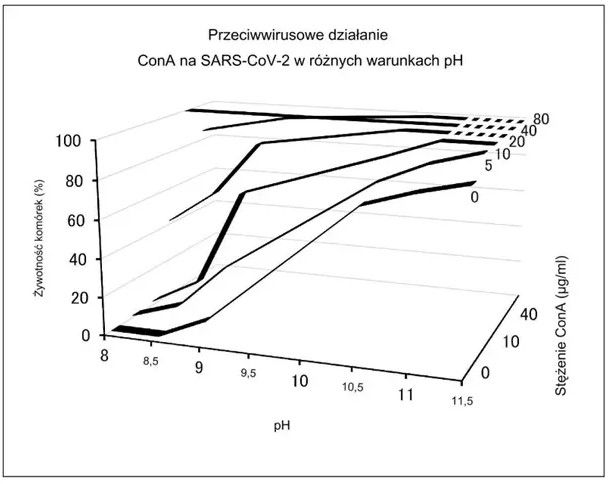
Rysunek 4. Wpływ ConA na SARS-CoV-2 w różnych warunkach pH.
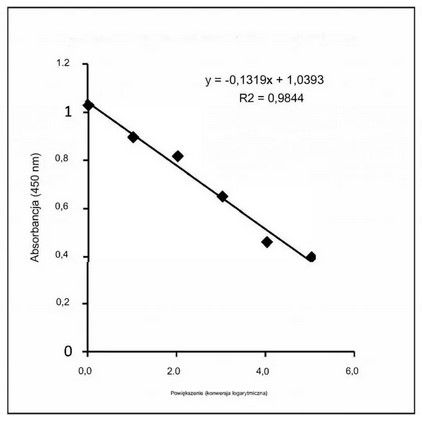
Rysunek 5. Krzywa kalibracji do obliczania zawartości ConA w proszku fasoli.
Dr. Seiya Sato posiada ponad 45 lat doświadczenia i ma kilkanaście zarejestrowanych światowych patentów dotyczących badań nad wirusami, w tym dotyczących sposobów ich wykrywania. Dr Sato jako pierwszy na świecie opracował zestaw do szybkiej diagnostyki antygenów grypy w 1995 roku (patent w JPO), kiedy był dyrektorem firmy Denka Seiken (Japonia). Wszystkie badania dotyczące wirusa zostały przeprowadzone w jego laboratorium oraz w laboratoriach innych jednostek naukowych i centrów badawczych współpracujących z nim w Niigata, Japonia.